
Život so sklerózou
Skleróza multiplex (SM) je chronické zápalové ochorenie centrálneho nervového systému, teda mozgu a miechy. Príčina ochorenia zostáva neobjasnená. Na imunitnú poruchu má vplyv genetika a faktory prostredia. Z týchto faktorov sa do súvislosti s ochorením najčastejšie dáva vplyv slnečného žiarenia, hladina vitamínu D, infekčné ochorenia, ale aj vplyv diéty, obezity a zloženia črevného mikrobiómu.
Väčšina lekárov nepovažuje diétu v liečbe sklerózy multiplex za dôležitú, neexistujú oficiálne odporúčania ohľadne zmeny stravovania pri SM, dokonca jej odporúčanie väčšina neurológov považuje za nevhodné, nanajvýš sa pacienti stretnú s vágnym odporúčaním, že sa majú zdravo stravovať. Ako by mohlo niečo tak jednoduché, ako to čo jeme, mať vplyv na tak záhadnú chorobu akou je skleróza multiplex?
Väčšina lekárov a vedcov očakáva, že jedného dňa sa nájde príčina tohto ochorenia v laboratóriu pomocou vysokosofistikovaného imunologického alebo genetického výskumu. Sú doteraz publikované výsledky štúdií vplyvu diéty na SM, na autoimunitné choroby a zápal dostatočne motivujúce pre Vás? Alebo Vás zaujímajú osudy pacientov, ktorí držia určitý typ diéty, a jej vplyv na priebeh ich ochorenia?
Na tejto stránke nájdete zrozumiteľne podané vedecké fakty a výsledky výskumu týkajúce sa vplyvu diéty na priebeh SM.
Celosvetový výskyt SM
Skleróza multiplex (SM) je chronické zápalové, demyelinizačné a sekundárne neurodegeneratívne ochorenie centrálneho nervového systému. Príčina ochorenia zostáva neobjasnená. Na imunitnú poruchu vplývajú genetické a environmentálne faktory. Z environmentálnych faktorov sa v patogenéze ochorenia najčastejšie skloňuje vplyv slnečného žiarenia, hladiny vitamínu D, infekčných patogénov, ale aj vplyv diéty, obezity a zloženia črevného mikrobiómu. Oficiálne odporúčania ohľadne zloženia diéty alebo užívania výživových doplnkov však všeobecne chýbajú. Americká národná spoločnosť pre SM (National Multipe Sclerosis Society) ale v priebehu posledného roka pripustila vo svojich odporúčaniach, že diéta so zníženým obsahom saturovaných tukov s pridaním omega-3 a omega-6 mastných kyselín môže mať priaznivý vplyv na priebeh SM.
Výskumy poukazujú na vplyv stravy na autoimunitu, z makronutrientov na imunitný systém najviac vplývajú tuky, príjem rôznych typov tukov môže mať buď pro- alebo protizápalový efekt. Potrava má i nezanedbateľný vplyv na zloženie črevného mikrobiómu, ktorý sa javí kľúčovým v patogenéze autoimnunitných ochorení. Z výživových doplnkov sa najčastejšie do súvislosti s SM dáva vitamín D, a i napriek tomu, že dôkaz vplyvu suplementácie vitamínom D na priebeh ochorenia chýba, sa táto pacientom rutinne odporúča.
Práca poskytuje prehľad existujúcich dôkazov z epidemiologických, klinických a laboratórnych štúdií o možnom a pravdepodobne významnom vplyve zloženia stravy na patogenézu SM, podrobne sa venuje štúdiám o vplyve zloženia tukov, obsahu esenciálnych mastných kyselín a vitamínu D v diéte pacienta s SM na priebeh ochorenia.
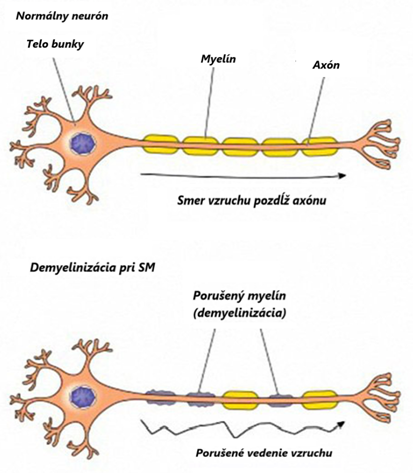
SM je najčastejším imunitne mediovaným ochorením CNS, postihujúce hlavne mladých ľudí, viac ženy ako mužov. Aberantná imunitná reakcia do rôznej miery poškodzuje myelín a neuróny CNS a ochorenie najčastejšie prebieha v atakoch, typicky v priebehu rokov zápalové ochorenie postihuje rôzne lokality CNS.
U Európanov a ich potomkov je SM najčastejšou príčinou netraumatického neurologického postihnutia mladých ľudí. Postihuje približne 2,5 milióna ľudí celosvetovo a vyše 400,000 dospelých len v USA.
Epidemiologické údaje vykazujú vyššiu prevalenciu SM v rozvinutých krajinách ďalej od rovníka, kde je častá vysokokalorická strava s vysokým obsahom tuku. Najvyššia prevalencia je v severnej Amerike a západnej Európe (140 a 108 na 100 000 obyvateľov) a najnižšia v subsaharskej Afrike a východnej Ázii (2,1 a 2,2 na 100 000 obyvateľov), tento fakt sa tradične vysvetľuje nižšou expozíciou slnečnému žiareniu v krajinách ďalej od rovníka, čo ale nekoreluje s veľmi nízkou prevalenciou SM napr. v Číne a Japonsku, ktoré ležia v porovnateľnej zemepisnej šírke. (Atlas of MS 2013)
Z historického hľadiska sa SM javí ako moderné ochorenie, podobne ako ateroskleróza sa objavuje v lekárskej literatúre až od 19. storočia a jej incidencia narastá. (Hollenbach, 2015)
Tento nárast sa zaznamenáva primárne u žien a u populácií tradične považovaných za nízko rizikové ako napr. Hispánci, Ázijci a Afroameričania. Štúdia amerických veteránov koncom 20. storočia zaznamenala nižšiu incidenciu SM u Afroameričanov, čo ale podobná štúdia z 21. storočia už nezaznamenáva. (Wallin et al, 2012)
Nárast incidencie SM ďalej dokumentujú epidemiologické štúdie z Austrálie (Barnett et al. 2003), Nórska (Grytten et al. 2015), Poľska (Brola et al. 2017), Kuvaitu (Alshubaili et al. 2005), Argentíny (Cristiano et al. 2016) a Japonska. V Japonsku, kde je prevalencia SM veľmi nízka, posledná štúdia poukazuje na 4- násobný nárast v prevalencii SM v roku 2003 (7,7/100 000) v porovnaní s rokom 1972. SM fenotyp sa zmenil ´westernizáciou´ a tzv. ´západný´ fenotyp SM je teraz v Japonsku častejší ako predtým sa vyskytujúca forma optiko-spinálnej SM. (Kira et al. 2008)
SM je chronické civilizačné ochorenie a do veľkej miery súvisí so životným štýlom.
Presná patogenéza a príčina ochorenia nie je úplne objasnená, mnohí odborníci pokladajú SM za záhadné ochorenie. Vieme však, že SM vzniká pri určitej genetickej predispozícii vplyvom vonkajších faktorov, mnohé z nich majú súvis so životným štýlom.
Predispozíciu k ochoreniu SM dedíme, nejde tu však o jednoduchý Mendelovský typ dedičnosti, uplatňuje sa tu génový polymorfizmus, jednotlivé rizikové alely génov sú v populácii relatívne časté a každá má malý efekt na celkové riziko.
Genómové asociačné štúdie (GWAS) doteraz odhalili viac ako 100 génových polymorfizmov – kažý prispieva k riziku SM len malu časťou, najviac mutácií je však v génoch HLA, ktoré súvisia s imunitným systémom. (Hollenbach et al, 2015)
Centrálnym bodom výskumu SM je hľadanie príčiny a mechanizmu vzniku zápalu v CNS. Za príčinu vzniku zápalového plaku, ktorý histopatologicky charakterizujete toto ochorenie, sa všeobecne považuje porušenie integrity hemato-encefalickej bariéry u geneticky predisponovanej osoby a porucha imunitných procesov.
Hemato-encefalická bariéra je hranicou medzi mozgom a krvou cirkulujúcou v jeho cievach, bunky ciev sú tak nepriepustné pre mnohé krvné elementy, napríklad leukocyty za normálnych okolností nie sú schopné prekonať túto bariéru. Hypoteticky sa predpokladá, že systémová infekcia, napríklad infekcia vírusom EBV, môže spôsobiť zvýšenú priepustnosť výstelky ciev mozgu a miechy, umožniť leukocytom prestúpiť cievnu stenu do normálne imunologicky privilegovaného CNS. Jedna štúdia popisuje i zvýšený výskyt SM u ľudí po traumatickom poškodení mozgu, pri ktorom pravdepodobne takisto vzniká porušenie hemato-encefalickej bariéry. Ak by v týchto bunkách prestupujúcich do mozgového tkaniva existovali leukocyty programované rozoznať myelínový antigén, môžu spustiť zápalovú kaskádu vedúcu k vzniku akútnej zápalovej demyelinizačnej lézie. Tieto lézie typicky vznikajú v bielej hmote, napádané sú hlavne bunky s myelínovou pošvou – oligodendrocyty, avšak sú popísané i lézie šedej hmoty, kde je atakovaný takisto myelín. (Frohman et al 2006)
Sclerosis multiplex podmieňuje zvýšená prozápalová aktivita početných buniek imunitného systému pod „vedením“ Th1- a najmä Th17-subpopulácie lymfocytov. V ostatnej dobe sa zistilo, že nadmernú prozápalovú aktivitu uvedených skupín lymfocytov umožňuje aj nedostatočná imunosupresívna aktivita T regulačných (Treg)-lymfocytov.
Existuje koncept ´inside-out´ patogenézy, ktorý suponuje, že SM začína ako primárna lézia CNS zapríčinená napr. infekciou alebo neurodegeneráciou, dochádza k uvoľneniu autoantigénov, voči ktorým reagujú autoreaktívne T a B lymfocyty. Naproti tomu ´outside-in´ koncept podporovaný výskumom EAE u laboratórnych zvierat predpokladá aktiváciu autoreaktívnych T lymfocytov periférnou infekciou. V oboch prípadoch aktivované CD4+ Th1 a Th17 bunky infiltrujú CNS a je prítomná jasná prevaha efektorových oproti regulatórnym bunkám.
V imunitnom systéme existuje rovnováha medzi prozápalovou (Th1) a protizápalovou odpoveďou (Th2)
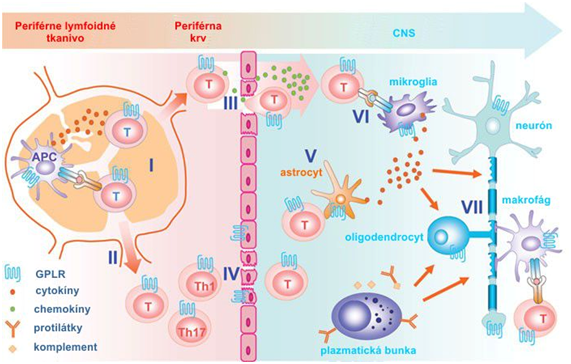
Obrázok: Imunopatogenéza pri SM: (I) aktivácia T-buniek, (II) T bunky migrujú z lymfoidného tkaniva, (III) migrácia zápalových buniek z periférie a infiltrácia CNS cez hemato-encefalickú bariéru, (IV) hematoencefalická bariéra, GPCR – receptor združený s G – proteínom, (V) aktivácia astrocytov, (VI) aktivácia mikroglie, (VII) demyelinizácia a neurotoxicita
Upravené podľa: Cell Research22(7):1108-28, 2012
Symptómy ochorenia
SM je zápalové demyelinizačné ochorenie, čo znamená že zápal poškodzuje myelín – tenkú tukovú vrstvu na povrchu nervových buniek CNS, teda mozgu a miechy. Zápal nepoškodzuje periférne nervy a ich myelínové obaly. Symptómy ochorenia závisia od toho, ktoré miesto zápal postihol a do akej miery. Často sú postihnuté očné nervy (optická neuritída- dočasná strata zraku postihujúca jedno oko), lebo majú hrubú myelínovú vrstvu alebo mozgové dráhy regulujúce očné pohyby v mozgovom kmeni (vzniká dvojité videnie).
Ďalšie časté príznaky sú:
- strata citlivosti, mravenčenie
- poruchy hybnosti, zvýšený tonus svalstva – spasticita, svalové kŕče
- porucha rovnováhy, reči, tremor – pri poškodení centier rovnováhy (mozoček, mozgový kmeň)
- bolesti tváre – neuralgia
- únava, bolesť
- subjektívne kognitívne ťažkosti, problémy s rozhodovaním, až demencia
- depresia, menej často eufória
- intolerancia tepla
Demyelinizačné zápalové lézie majú tendenciu sa reparovať – prebieha remyelinizácia a úprava myelínu, táto však väčšinou nebýva úplná a v CNS sa tvoria jazvy. U pacienta dochádza k zmierneniu alebo úplnému vymiznutiu príznakov. Ak symptómy nevymiznú úplne, majú tendenciu pretrvávať a ich stupeň varíruje, napr. sa zhoršia po námahe, v teple, pri inom ochorení. Zhoršenie neurologických príznakov napríklad pri zahriatí sa pri cvičení je normálnym javom, nemalo by pacientov odradiť od cvičenia. Ak zápal postihne tzv. tiché miesta mozgu – nemusí sa prejaviť žiadnymi príznakmi, len novými léziami na MR vyšetrení.
SM, príčina ochorenia
Presná príčina ochorenia nie je objasnená. Vieme, že na vznik ochorenia má vplyv genetika a vplyvy prostredia, a že sa jedná o autoimunitné zápalové ochorenie, t.j. ochorenie, kde je zápal vyvolaný dysreguláciou vlastného imunitného systému. Centrálnym bodom výskumu SM je hľadanie príčiny a mechanizmu vzniku zápalu CNS/plaku. Za príčinu vzniku zápalu CNS sa všeobecne považuje porušenie integrity hemato-encefalickej bariéry u geneticky predisponovanej osoby a porucha imunitných procesov, t,j, vlastným imunitným bunkách sa podarí dostať do CNS kde vyvolajú zápal.
Z environmentálnych faktorov, ktoré sa považujú za spúšťače ochorenia a priamych aktivátorov atakujúcich imunitných buniek sa najčastejšie citujú vírusové a iné mikrobiálne agens. Početné vírusy obsahujú proteíny, ktoré majú príbuznú štruktúru s hlavným autoantigénom pri SM – myelínovým bázickým proteínom (MBP). Ide o vírus osýpok, CMV, EBV, HBV, HSV, humánny herpetický vírus 6 alebo 7, koronavírusy a iné. Vzťah medzi vírusmi a SM podporujú aj údaje, že vírusové infekcie často predchádzajú ataku ochorenia. K ďalším environmentálnym faktorom, ktoré majú dokázaný vplyv na výskyt SM, patrí deficiencia vitamínu D, fajčenie a obezita.
Výskum poukazuje na vplyv diéty na autoimunitu, z makronutrientov na imunitný systém najviac vplývajú tuky. Príjem rôznych typov tukov môže mať buď pro- alebo protizápalový efekt. Strava má i nezanedbateľný vplyv na zloženie črevného mikrobiómu, ktorý sa javí kľúčovým v patogenéze autoimnunitných ochorení.